ADC & Biokonjugation

Bei der Biokonjugation werden Moleküle miteinander verknüpft, wobei mindestens einer der Reaktanten ein Biomolekül ist. Häufig handelt es sich dabei um einen Antikörper, ein Protein oder Oligonukleotid. Verwendet werden Biokonjugate zum Nachweis, zur Analyse oder zum Targeting und Tracking von Biomolekülen in der Biotechnologie, Medizin und Nanotechnologie. Zu den Anwendungen gehören das Anheften von Fluoreszenz-Sonden an Antikörper für die Durchflusszytometrie und die mikroskopische Bildgebung, das Anheften von Antikörpern an Beads für Immunpräzipitationen, das Anheften von Antikörpern an Wirkstoffe für die Arzneimittelentwicklung und das Vernetzen von Proteinen zur Ermittlung ihrer biologischen Wechselwirkungen.
Bei der Antikörper-Wirkstoff-Konjugation (ADC) werden monoklonale Antikörper verwendet, um hochaktive oder potente pharmazeutische Wirkstoffe (HPAPI) zielgerichtet zu den gewünschten Zellen zu transportieren. In konjugierter Form weisen die HPAPI eine selektivere therapeutische Aktivität auf und verschonen Nicht-Zielzellen. Diese Biokonjugationstechnik wird für den gezielten und sicheren Wirkstofftransport eingesetzt. Entscheidend für die Auswahl der Vernetzungsreagenzien und Reaktionsmethoden für eine optimale Biokonjugation sind chemische und physikalische Eigenschaften, Länge, Molekülgröße, Mischbarkeit mit Wasser und Spaltbarkeit des Reagens, Anwendungskriterien sowie die zu vernetzenden funktionellen Gruppen.
Ausgewählte Kategorien
Entdecken Sie unsere Auswahl an Polyethylenglykol (PEG) und PEG-Derivaten mit einem breiten Spektrum an ...
Hochwertige Aminosäuren, Harze und Reagenzien, einschließlich Novabiochem® für die Peptidsynthese ...
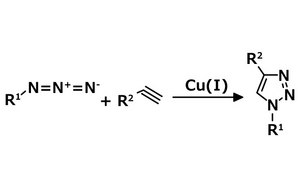
Click-Chemie-Reagenzien beschleunigen den Fortschritt in der chemischen Biologie, Biokonjugation und ...
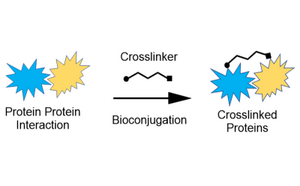
Linker und Crosslinker bieten strukturelle Stabilität bei der Biokonjugation für Protein-Protein-, Protein-Peptid- und Peptid-Kleinmolekül-Interaktionen.
Vernetzertypen in der Biokonjugation
Einer der grundlegendsten Aspekte bei der Entwicklung von Vernetzern ist die Frage, ob das Reagenz homobifunktionell oder heterobifunktionell ist. Die überwiegende Mehrheit der Biokonjugat-Reagenzien ist bifunktionell, d. h. zwei reaktive Gruppen befinden sich in der Regel an den äußeren Enden eines organischen Spacers. Bei einer homobifunktionellen Verbindung sind die beiden reaktiven Gruppen identisch, während sie bei einer heterobifunktionellen Verbindung unterschiedlich sind. Heterobifunktionelle Reagenzien haben gegenüber homobifunktionellen Reagenzien große Vorteile bei der Bildung von Biokonjugaten, da eine reaktive Endgruppe nur mit einer bestimmten funktionellen Gruppe koppelt, während die andere reaktive Endgruppe mit einer anderen funktionellen Gruppe reagiert.
Vernetzerlänge in der Biokonjugation
Es ist wichtig, bei der Auswahl eines Vernetzers oder Modifikationsreagens für die Konjugationsreaktion die Abmessungen oder die lineare Gesamtlänge des Zielmoleküls vor und nach der Konjugation zu berücksichtigen. Die molekulare Länge der entstehenden Verbindung wird hauptsächlich durch den Spacer-Arm – auch als Crossbridge (Querbrücke) bezeichnet – des Reagens bestimmt. Vernetzer unterschiedlicher Größe werden so zu molekularen Maßstäben für die Messung der Abstände zwischen funktionellen Gruppen in Biomolekülen.
Spaltbare vs. nicht spaltbare Biokonjugationsvernetzer
Es ist wichtig, dass der Vernetzer spaltbar ist, wenn die interagierenden Biomoleküle isoliert und analysiert werden müssen, z. B. bei einem Vernetzer, der zum Nachweis von Protein-Protein-Wechselwirkungen verwendet wird. Wenn Stabilität erforderlich ist, kann alternativ ein nicht spaltbarer Linker verwendet werden, z. B. ein Antikörper, der an ein Harz für das Einfangen (Capture) von Proteinen gebunden ist.
Hydrophobe vs. hydrophile Biokonjugationsvernetzer
Bei manchen Anwendungen kann die Hydrophobie des Reagens von Vorteil sein – vor allem dann, wenn eine Anwendung das Durchdringen der Zellmembranen erfordert. Hydrophobe Reagenzien ohne stark polare Gruppen passieren schnell die Zellmembranen, um zellinterne Proteine zu vernetzen oder zu markieren. Andererseits verursachen hydrophile Vernetzer keine Aggregation oder Ausfällung des interagierenden Moleküls und können zu einer Wasserlöslichkeit von Antikörpern und Proteinen führen, die durch sie modifiziert wurden. Die Verwendung von hydrophilen Biokonjugationsreagenzien führt auch zu einer besseren Biokompatibilität.
Funktionelle Gruppen als Ziel in der Biokonjugation
Die reaktionsfreudigsten funktionellen Gruppen in Biomolekülen stehen mit den Heteroatomen N, O und S in Verbindung, die aufgrund eines nicht geteilten Elektronenpaars nukleophil sind und spontan mit den kompatiblen und elektrophilen aktiven Gruppen von Vernetzern und Modifizierungsreagenzien reagieren können. In vielen Fällen sind die nukleophilen funktionellen Gruppen in Biomolekülen frei und zugänglich. In einigen Fällen werden sie jedoch erstellt, um Reaktivität und Kopplung zu ermöglichen. Es gibt mehrere spezialisierte Reagenzien, die die Erstellung einer geeigneten funktionellen Gruppe für die Biokonjugation erleichtern, falls das gewünschte Reagenz nicht verfügbar ist. Die natürlich vorkommenden funktionellen Gruppen in Biomolekülen sind Amine, Thiole, Hydroxylgruppen, Carboxylate, Aldehyde, organische Phosphate und reaktive Wasserstoffe an bestimmten aktivierten Kohlenstoffatomen.
Entwicklung und Herstellung von ADC
Die Entwicklung eines Antikörper-Wirkstoff-Konjugats (ADC) erfordert Expertise in der Entwicklung, Herstellung, Formulierung und Prüfung kleiner und großer Moleküle. Die Wahl eines erfahrenen Partners, der über diese Fähigkeiten und die erforderlichen Containment-Einrichtungen verfügt, kann Sie dabei unterstützen, Ihr ADC bis zur Marktreife zu bringen. ADC sind herausfordernde Moleküle und erfordern modernste Produktionsanlagen sowie spezielle Ausrüstung, um das Molekül zu charakterisieren und seine Reinheit, Homogenität und Stabilität nachzuweisen.
Besuchen Sie unsere Dokumentensuche, wo Sie Datenblätter, Zertifikate und technische Dokumentation finden.
Zugehörige Artikel
- Drug discovery process by utilizing chemistry reaction of Cu(I)-catalyzed Huisgen 1,3-dipolar cycloaddition of terminal alkynes with organoazides to yield 1,4-disubstituted 1,2,3-triazoles.
- Click chemistry is an approach to the synthesis of drug-like molecules that can accelerate the drug discovery process by using a few practical and reliable reactions.
- Copper-free click chemistry is an alternative approach to click chemistry that proceeds at a lower activation barrier and is free of cytotoxic transition metal catalysts.
- Originally reported by Staudinger and Meyer, azides react readily with triarylphosphines to form the corresponding iminophophoranes. The Staudinger Ligation: A High-Yield, Chemoselective, and Mild Synthetic Method.
- Alle anzeigen (17)
Mehr Artikel und Protokolle finden
Wie wir weiterhelfen können
Sollten Sie Fragen haben, reichen Sie bitte eine Anfrage beim Kundensupport
ein oder sprechen Sie mit unserem Kundenservice:
E-Mail custserv@sial.com
oder telefonisch unter +1 (800) 244-1173
Weitere Unterstützung
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- Rechner & Apps
Web-Toolbox - wissenschaftliche Forschungstools und Informationsquellen für die Bereiche analytische Chemie, Life Science, chemische Synthese und Materialwissenschaft.
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
Um weiterzulesen, melden Sie sich bitte an oder erstellen ein Konto.
Sie haben kein Konto?