펩타이드 합성
펩타이드는 아미드 결합을 통해 연결된 두 개 이상의 아미노산으로 구성되며, 일반적으로 2~70개의 아미노산으로 이루어진 아미노산 사슬을 형성합니다. 펩타이드는 생물학적 활성을 나타내기 위한 접힘 구조가 필요 없어 단백질과 구별됩니다. 펩타이드는 내생적으로 angiotension, LHRH, 엔케팔린과 같은 펩타이드 호르몬으로 나타나며, 동물과 식물에서 독소가 펩타이드 형태로 발견됩니다. 펩타이드는 약물 개발을 위한 선도물질 화합물로서 또한 그 자체로 약물로서 큰 관심을 끌고 있습니다. 또한 백신, 생체 재료, 조직학적 프로브에 응용되며, 항체를 생성하기 위한 항원으로서 많은 수의 펩타이드가 사용됩니다.
펩타이드는 용액 또는 고체 상태에서 화학적으로 합성됩니다. 이 과정은 N-보호된 아미노산과 유리 아미노기와 보호된 카복실산을 가진 아미노산 사이의 직접적/선택적 아미드 결합에 의해 형성됩니다. 고체상 합성에서, 카복실 보호기는 폴리머 지지체에 연결됩니다. 결합 형성 후, 다이펩타이드의 아미노 보호기가 제거되고, 다음 N 보호 아미노산이 결합됩니다.
주요 카테고리
당사의 안정적이고 허용 가능한 NHC 리간드 및 복합체는 유기금속 촉매 및 촉매 화학 연구에서 워크플로우를 유지하기 위한 효율적인 보조 리간드로 사용될 수 있습니다.
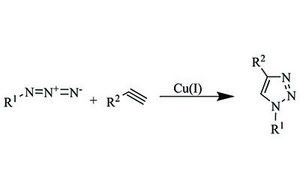
자사의 클릭(Click) 화학 시약 포트폴리오에는 다양한 아자이드, 알카인, 촉매 및 리간드가 포함되어 있어 화학 생물학, 고분자 화학, 생체접합 및 약물 발견의 발전을 가속화합니다.
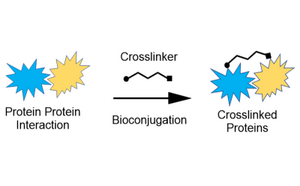
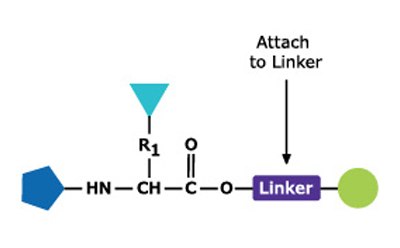
자사의 링커(Linker) 및 가교제(Crosslinker) 포트폴리오는 모든 귀하의 생체접합 요구를 위해 단백질-단백질, 단백질-펩타이드 및 펩타이드/단백질-저분자 상호 작용에서 구조적 안정성 및 신뢰성을 제공합니다.
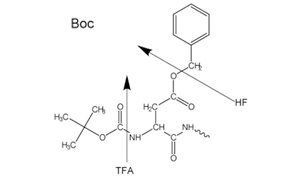
Figure 2Side-chain protecting groups for Boc solid-phase peptide synthesis (SPPS)
고체상 펩타이드 합성(SSPS)은 효율성, 단순성, 속도, 병렬화 용이성 때문에 가장 자주 사용되는 펩타이드 합성 방법입니다. SSPS는 불용성 중합체 지지체에 부착된 아미노산 또는 펩타이드에 아미노산 및 측면 보호 아미노산 잔기를 순차적으로 추가합니다(그림 1).
N-α 보호에 산성 라벨 Boc 잔기(Boc SPPS) 또는 염기 라벨 Fmoc 잔기(Fmoc SPPS)가 사용됩니다. 이 보호기를 제거한 후, 결합 시약 또는 사전 활성화된 보호된 아미노산 유도체를 사용하여 그 다음 보호된 아미노산을 추가합니다. C 말단 아미노산은 링커를 통해 레진에 고정되며, 링커의 특성은 사슬 확장 후 펩타이드를 지지체로부터 방출하는 데 필요한 조건을 결정합니다. 측면 사슬 보호기는 종종 레진으로부터 펩타이드를 분리하여 동시에 절단되도록 선택됩니다(그림 2와 3).
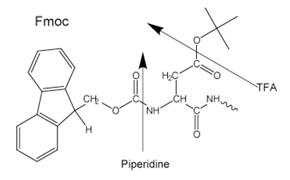
Figure 3.Side-chain protecting groups for Fmoc solid-phase peptide synthesis (SPPS)
대부분의 펩타이드는 Fmoc 방법을 사용하여 준비되며, 마지막 단계의 절단 및 탈보호화는 특수 장비에서 고도로 독성이며 부식성인 무수 HF 액체를 사용해야 하는 Boc 방법과 대조됩니다.
100 아미노산 이상의 단백질 합성이 일반적으로 보고되지만, 50개의 아미노산으로 이루어진 펩타이드는 루틴하게 제조될 수 있습니다. 더 긴 단백질은 용액에서 완전히 탈보호된 펩타이드의 화학적 결찰로 만들어질 수 있습니다. 이 기법을 사용하면 박테리아에서 발현하기 어려운 천연 펩타이드를 합성하고, 비천연 또는 D-아미노산을 통합하며, 고리형, 분지형, 표지형 및 번역 후 변형 펩타이드를 생성할 수 있습니다.
액체 상태 펩타이드 합성은 보통 Boc 또는 Z-아미노 보호를 활용하며, 산업적 목적을 위한 대규모 펩타이드 합성 과정을 제외하고는 고체 상태 펩타이드 합성에 의해 대체되었습니다.
관련 자료
- Novabiochem® has one of the most extensive ranges of linkers and derivatized resins for Fmoc solid phase peptide synthesis. These resins have varied properties with special protocols for loading and cleaving.
- Chromogenic and fluorogenic derivatives are invaluable tools for biochemistry, having numerous applications in enzymology, protein chemistry, immunology and histochemistry.
- Aspartimide formation 1,2 is caused by repeated exposure of aspartic acid-containing sequences to bases like piperidine and can result ultimately in the generation of 9 different by-products.
- The Novabiochem® product line has one of the most extensive ranges of polymer-supports for solid phase peptide synthesis. They range from high-loaded, lows welling for the large-scale production of relatively short peptides to high-swelling, low-loaded for the synthesis of long or difficult sequences.
- Our long peptide purification utilizes a combination of chemoselective purification tags and standard RP-HPLC. The method is especially effective at removing impurities that are closely eluting or hidden under the isolated product peak
- 모두 보기 (22)
관련 프로토콜
- A guide to create solvent systems used for the thin-layer chromatography assay of Novabiochem products.
- Overcome challenges in synthesis and disulfide bond formation with protocols for Fmoc solid-phase peptide synthesis of peptides with cysteine and methionine.
- Amide Coupling in a Box
- Information on the Amide bond and the Catalytic Amide Bond Formation Protocol. Amidation of amines and alcohols. The amide bond, an important linkage in organic chemistry, is a key functional group in peptides, polymers, and many natural products and pharmaceuticals.
- We provide an overview of our available reagents, together with recommendations and details of their use for synthesis of peptides containing post-translationally modified amino acids.
- 모두 보기 (10)
더 많은 관련 문서와 프로토콜을 찾아보세요.
저희가 도와드리겠습니다
문의 사항이 있으시면 고객 지원 요청서를 제출하시거나
또는 당사 고객 서비스 팀에 말씀해 주십시오.
이메일 custserv@sial.com
또는 전화 +1 (800) 244-1173
추가 지원
- Chromatogram Search
Use the Chromatogram Search to identify unknown compounds in your sample.
- 계산기 및 앱
웹 툴박스 - 분석 화학, 생명과학, 화학 합성 및 재료 과학을 위한 과학 연구 도구 및 리소스.
- Customer Support Request
씨그마 알드리치의 주문, 제품, 계정 및 웹사이트에 대해 궁금하신 부분을 확인할 수 있습니다
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
계속 읽으시려면 로그인하거나 계정을 생성하세요.
계정이 없으십니까?