Virus-Based Vaccine Manufacturing
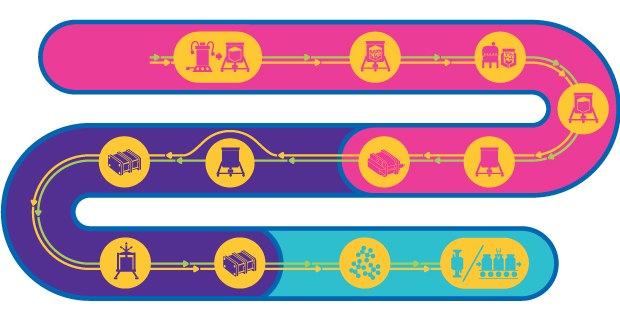
Đào tạo quy trình cho cả vi-rút không hoạt động và vi-rút đã suy giảm trực tiếp
Vắc-xin dựa trên vi-rút bao gồm virus suy giảm hoặc bất hoạt. Những vắc-xin này có thể kích hoạt tất cả các giai đoạn của hệ thống miễn dịch và cung cấp khả năng miễn dịch lâu dài và nhanh chóng bằng cách gợi ra các kháng thể trung hòa chống lại mầm bệnh đích.
Quá trình sản xuất vắc-xin dựa trên virus bị suy giảm rất phức tạp, bao gồm nhiều bước và phải duy trì khả năng lây nhiễm của virus đã suy giảm. Mặc dù có quy trình sản xuất chung, phương pháp tiếp cận mẫu cho sản xuất không tồn tại. Thay vào đó, mỗi quy trình phải được điều chỉnh dựa trên hình dạng, kích thước, bản chất, hành vi hóa học physico, sự ổn định, và tính đặc hiệu của virus.
Featured Categories
Dòng lò phản ứng sinh học Mobius ® cung cấp các lò phản ứng sinh học sử dụng một lần để nuôi cấy tế bào từ khi phát triển ban đầu đến sản xuất thương mại, hỗ trợ nhiều quy mô khác nhau.
Các sản phẩm đa phương tiện nuôi cấy tế bào (CCM) có thể tùy chỉnh và sẵn có thể tùy chỉnh của chúng tôi nâng cao năng suất trong các quy trình mAb ngược dòng, vắc-xin, gen/liệu pháp tế bào.
Bộ lọc độ sâu phần cứng linh hoạt và dùng một lần tạo điều kiện cho việc làm rõ quy mô quy trình và thử nghiệm, cho phép nâng cấp theo mô-đun và mở rộng quy mô.
Các hệ thống dây chuyền sản xuất sẵn sàng sử dụng, ngoài kệ của chúng tôi giúp giảm đáng kể thời gian, chi phí và rủi ro phát triển dây chuyền sản xuất mới. Cho dù bạn đang sản xuất kháng thể, protein tái tổ hợp, vắc-xin hoặc vector virus để điều trị gen, nền tảng dòng tế bào của chúng tôi có thể đẩy nhanh tiến trình ngược dòng của bạn.
Tối ưu hóa năng suất ngược dòng và làm rõ với khả năng nâng cấp đáng tin cậy
Các quy trình nuôi cấy ngược dòng được phát triển để sản xuất vắc-xin dựa trên virus phải được tối ưu hóa để đáp ứng các yêu cầu về năng suất. Tối ưu hóa này bao gồm bước làm rõ cần thiết để loại bỏ tế bào và mảnh vụn tế bào và để đảm bảo thu hoạch virus mạnh mẽ. Quá trình thượng nguồn chỉ thành công, tuy nhiên, nếu nó có thể được thu nhỏ đáng tin cậy để đáp ứng nhu cầu thị trường dự kiến.
Đạt được mục tiêu hiệu suất và năng suất với khả năng loại bỏ tạp chất mạnh mẽ
Axit nucleic từ các tế bào phân ly là một chất gây ô nhiễm phổ biến trong các quá trình vắc-xin dựa trên virus. Các quy định yêu cầu mức độ axit nucleic của tế bào chủ phải dưới 10 ng/liều vắc-xin dựa trên virus suy giảm. Xử lý endonuclease Benzonase ®, sau đó lọc dòng tiếp tuyến là sự kết hợp mạnh mẽ và mạnh mẽ để phân hủy và sau đó loại bỏ các thành phần axit nucleic còn lại.
Tối đa hóa phục hồi hạ nguồn
Điều trị endonuclease Benzonase ® là đủ để đạt được mức độ tinh khiết mong muốn đối với hầu hết các loại vắc-xin dựa trên virus trong quá trình tập trung vầ diafiltration. Tuy nhiên, sắc ký là cần thiết để đạt được mục tiêu tinh khiết cho các loại vắc-xin dựa trên vi-rút thế hệ tiếp theo như virus viêm não Nhật Bản (JEV) và virus sốt xuất huyết (DENSO). Bởi vì mỗi quy trình sản xuất phải được điều chỉnh phù hợp với các đặc tính của virus, một hộp công cụ tùy chọn để tinh chế xuôi dòng là điều cần thiết để mang lại độ tinh khiết mong muốn trong khi đảm bảo phục hồi tối ưu.
Đảm bảo an toàn cho bệnh nhân
Mặc dù vắc-xin dựa trên vi-rút được sản xuất bằng cách sử dụng virus suy giảm, đảm bảo sự an toàn của bệnh nhân vẫn là một mối quan tâm quan trọng. Số lượng lớn vắc-xin virus cuối cùng tương đương với lượng nước. Như vậy, vắc-xin có thể được khử trùng bằng cách lọc khử trùng 0,22 µm trước khi hoàn thành công thức cuối cùng và lấp đầy các bước hoàn thành.
Xử lý nuclease & làm rõ
Đảm bảo khả năng mở rộng mạnh mẽ:
- Xử lý nuclease bằng Benzonase® phù hợp cho sản xuất dược phẩm sinh học EMPROVE® Bio
- Phát hiện Benzonase ® với Benzonase® Elisa Kit II để phát hiện chất còn sót lại của endonase Benzonase ® trong quá trình này
- Làm rõ chính/phụ với Bộ lọc độ sâu LÕI Millistak+ ® HC
- Làm rõ chính với Bộ lọc độ sâu Clarisolve ®
- Làm rõ thứ cấp với băng Polysep II.
- Làm rõ thứ cấp với bộ lọc Cá nhân có Ảnh hưởng Chính trị Milligard ®
Môi trường & dung dịch đệm nuôi cấy tế bào lỏng xử lý sinh học
Chúng tôi cung cấp khả năng lọc chất lỏng vô trùng chất lượng cao nhất trong ngành, cung cấp phương tiện nuôi cấy tế bào, bộ đệm, CIP và các sản phẩm SIP từ các cơ sở GMP trên toàn thế giới để tối ưu hóa sản xuất biopharma của bạn.

Downstream - Lọc lưu lượng tiếp tuyến
Đạt được các mục tiêu về năng suất, hiệu quả và phục hồi vi-rút đồng thời đảm bảo loại bỏ tạp chất mạnh mẽ.
Downstream - Chromatography
- Sắc ký màng với nhựa Eshmuno ® Q
- Sắc ký màng với màng sắc ký mini Natrix ® Q Recon
- Sắc ký màng với màng sắc ký Natrix ® Q Pilot
- Chụp và/hoặc đánh bóng sắc ký bằng nhựa sắc ký Fractogel ® EMD DEAE
- Chụp và/hoặc đánh bóng sắc ký bằng nhựa sắc ký Fractogel ® EMD DMAE
- Giải pháp Mobius ® FlexReady cho chụp sắc ký

Lọc & nạp vô trùng lần cuối
Loại bỏ các mối quan ngại về ô nhiễm sản phẩm chéo đồng thời hợp lý hóa các yêu cầu hoàn thiện đổ đầy và tuân thủ các yêu cầu quy định hiện hành.
Phân tích Phần mềm & Công nghệ PAT
Truy cập phần tìm kiếm tài liệu của chúng tôi để tìm bảng dữ liệu, chứng chỉ và tài liệu kỹ thuật.
Bài viết liên quan
Tài nguyên liên quan
- Application Guide: Biopharmaceutical
A search tool to help you overcome your manufacturing challenges.
- Brochure: Vaccine Bioprocessing Handbook
In this handbook, we explain the vaccine production processes and process improvements for all types of vaccine development platforms.
- Mini-Handbook: Cell-Based Vaccine Bioprocessing
Live attenuated viral vaccines can be created using a complex, multi-step cell-based manufacturing process. It is not a templated process. The manufacturing process for each viral vaccine is different.
- e-Book: Enabling Capabilities & Solutions for all Vaccine Platforms
From process development to full-scale GMP-manufacturing, our global vaccine capabilities can help you achieve these goals for all your modalities/platforms including virus-based, subunit, VLP, viral vector, pDNA and mRNA vaccines.
- White Paper: Filtration Strategies for Optimal Development and Purification of a Foot and Mouth Disease Virus
We collaborated with MEVAC to optimize upstream and downstream processes for FMD vaccine manufacturing to establish a scalable, cost-efficient and GMP compliant process. This white paper focuses on the integration of new filtration strategies in both upstream and downstream processes.
- White Paper: Downstream Process Intensification for Virus Purification Using Membrane Chromatography
This white paper provides an overview of the challenges presented by current approaches to virus production and the opportunities to develop a platform approach that can work across different viral modalities and accelerate process development.
- Application Note: Effect of Benzonase® Endonuclease Addition to Purification of Sabin Polio Virus Type 3
This application note summarizes the benefits of incorporating Benzonase® endonuclease in a polio virus type 3 production process.
- Article: Filter-Based Clarification of Viral Vaccines and Vectors
In this article, a comprehensive overview is provided on different filtration technologies and their application in viral vaccine clarification, outlining challenges and present current best practices.
Tìm thêm Bài viết và Giao thức
How Can We Help
Trong trường hợp có bất kỳ câu hỏi nào, vui lòng gửi yêu cầu hỗ trợ khách hàng
hoặc trao đổi với nhóm dịch vụ khách hàng của chúng tôi:
Email custserv@sial.com
hoặc gọi +1 (800) 244-1173
Additional Support
- Calculators & Apps
Web Toolbox - science research tools and resources for analytical chemistry, life science, chemical synthesis and materials science.
- Customer Support Request
Customer support including help with orders, products, accounts, and website technical issues.
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
Để tiếp tục tìm hiểu, vui lòng đăng nhập hoặc tạo tài khoản.
Không có tài khoản?






