第I相、第II相

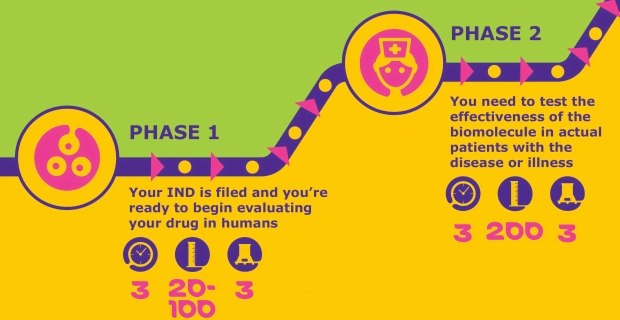
新薬治験開始申請(IND)が受領されたら、第I相試験を開始することができます。この開発段階では、健康な被験者を対象に薬剤候補物質の安全性が検討されます。
この段階で薬剤の製造能力の開発、標準化およびスケールアップを行い、適切な分析方法と品質管理プロセスに所定の標準化された能力があることを確認します。
薬剤候補物質の安全性が確立されたら、第II相試験で有効性を評価します。この段階の試験に成功することで、パートナーや投資家の関心を寄せることができます。この段階では、プロセスのスケールアップとさらなる最適化、ならびにエンドトキシン規格と無菌性の適合規を重点的に行います。
注目のカテゴリ
メルクのバイオ医薬品製造用細胞株は、新たな細胞株開発にかかる時間、コスト、リスクを大幅に削減します。抗体、組換えタンパク質、遺伝子治療用のウイルスベクターの生産に適したメルクの細胞株は、アップストリームプロセスの進捗を加速します。
臨床試験スケールの製造プロセスの開発および実施は複雑で、多大な時間がかかることがあり、多くのコンポーネントの仕様の要求と調達、全てを統合してプロセスの立ちあげが必要となります。臨床スケールテンプレートを使用すると、前臨床、フェーズ I、フェーズ II の減量を製造するための独自機能をすばやく確立できます。
以下のバイオ医薬品アプリケーション ガイドでテンプレート化されたプロセスについて詳しく説明します。
- ワクチン(mRNAなど)
- モノクローナル抗体(mAb)
- 抗体薬物複合体(ADC)
- 微生物
- プラスミドDNA(pDNA)
- 細胞・遺伝子治療(CGT)
適切なリソースを利用すれば、必要とする患者さんに有用である可能性が最も高い臨床的薬剤候補物質の発見に集中することができます。立ち上げ時にすぐに利用できるリソースについては、詳細を学ぶべき開発プロセスの段階を選定する、もしくは製品およびサービスのリンク先をご覧ください。
バイオテクノロジーハブリソースのワークフロー


創薬
新たな医薬品の開発に必要な検討事項、リソース、およびサポート

前臨床
治験薬(IND)申請のための安全性および有効性の立証

第III相・製造
治験および商品化に向けたスケールアップおよび技術移管から高品質生産までの発展

スタートアッププログラム
お客様の医薬品の可能性を広げるリソースと承認プログラムの連結

規制
世界で最も厳格な規制を有する産業への挑戦は信頼されているガイドとともにはじまります。
バイオテックリソース
- Biopharmaceutical Application Guide
Navigate the biopharmaceutical landscape with our application guide, providing resources and solutions for mAb, ADC, and mRNA processes.
- A Molecule’s Journey: Breaking Down Roadblocks to Clinical Success
A guidebook for biopharma executives navigating the complexities of clinical development. Learn how to successfully bring a molecule from the lab to the clinic.
- Quality and Regulatory Trends
Explore how we ensure high-quality products and services with a focus on compliance, risk management, and a strong code of conduct.
- Using a 3L Disposable Bioreactor to Increase Your Throughput Development Capacity
This webinar showcases the efficiency and economy of single-use bioreactors. Discover how using a 3L single-use bioreactor can enhance your throughput development capacity in therapeutic protein process development.
- Biosimilar Upstream Process Development – The Challenges and Promises
Explore the challenges and promises of biosimilar upstream process development. Learn how process changes impact product quality and achieve consistency in manufacturing.
- Mobius Single-Use Bioreactors Scalability: Bench to Clinical Scale
Discover how Mobius® Single-use Bioreactors enhance throughput development capacity, offering scalable solutions from bench to clinical scale.
お問い合わせ
ご不明な点がございましたら、お問い合わせページをご覧いただくか
、テクニカルサービスまでお問い合わせください。
メール:jpts@merckgroup.com
電話:03-6756-8245
サポート
- 計算ツール・アプリ
ウェブツールボックス-分析化学、ライフサイエンス、化学合成および材料科学のためのサイエンスリサーチツールとリソース
- Customer Support Request
お問い合わせページでは、製品のお問い合わせや、注文や納期、お取引やアカウント、ウェブサイトに関するお問い合わせをお申込みいただけます。
- FAQ
Explore our Frequently Asked Questions for answers to commonly asked questions about our products and services.
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?
